乐明药业洛索洛芬钠凝胶贴膏获批,九典制药市场格局生变
AI导读:
乐明药业洛索洛芬钠凝胶贴膏正式获批上市,成为首家视同通过一致性评价获批的该类产品,打破了九典制药长期独占的市场格局,引发市场广泛关注。
国家药品监督管理局近日宣布,乐明药业的洛索洛芬钠凝胶贴膏(CYHS2301270)正式获批在国内上市,成为“首家视同通过一致性评价获批”的该类产品。这一消息标志着长期由九典制药(300705.SZ)独家占据的市场份额被成功打破。
财联社记者尝试联系乐明药业以了解其市场推广计划,但多次拨打其官网电话均未得到回应。九典制药董事会秘书办公室则对此表示,公司不会对此事作出回应。
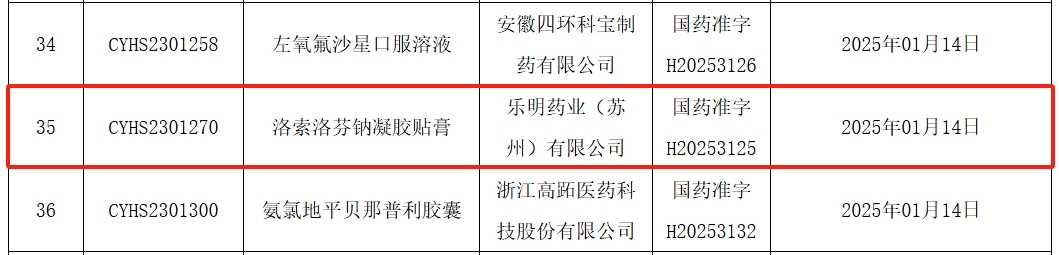
(图片来源:国家药品监督管理局网站)
早在1月15日,市场已流传乐明药业洛索洛芬钠凝胶贴膏获批的消息,导致九典制药股价当天收跌9.86%,报15.73元/股。随后的两个交易日,九典制药股价继续收跌,分别下跌1.46%和1.55%。
自2017年上市以来,九典制药的洛索洛芬钠凝胶贴膏一直是其核心收入来源。财报显示,2022年和2023年,该产品分别实现销售收入13.03亿元和15.47亿元,占公司整体营收的56.02%和57.46%。2024年前三季度,该产品实现销售收入11.69亿元,约占公司整体营收的54.47%。
乐明药业产品的获批引起了九典制药投资者的广泛关注。在1月16日的投资者交流会上,投资者围绕洛索洛芬钠凝胶贴膏提出了多个问题,但九典制药未直接回应,而是援引摩熵医药的数据指出,2023年外用贴膏剂市场销售规模约203.64亿元,其中医院端占比69.89%,零售端占比30.11%。
对于市场空间评估的问题,九典制药表示,由于其产品是独家品种,无法直接评估单品市场空间。据药融云数据,九典制药的洛索洛芬钠凝胶贴膏在2022年和2023年全国医院销售(全终端)的市场份额占有率均为100%。然而,九典制药透露,2025年已针对院外市场设定初步销售目标,计划重点推广包括洛索洛芬钠凝胶贴膏在内的3款贴膏剂。
“目前,我们已与全国排名前200的连锁药店建立了合作关系。”九典制药企业人员表示,但拒绝透露今年院外市场的单品销售提升计划。
资深医药行业专家郭新峰认为,洛索洛芬钠凝胶贴膏的市场尚未饱和,乐明药业产品的获批上市将与九典制药共同拓展市场空间。
药物临床试验登记与信息公示平台信息显示,乐明药业仅有一款洛索洛芬钠凝胶贴膏完成了临床试验,编号为“CTR20223303”。该临床试验为在中国健康受试者中进行的空腹给药条件下随机、开放、单剂量、两序列、两周期、双交叉生物等效性试验。
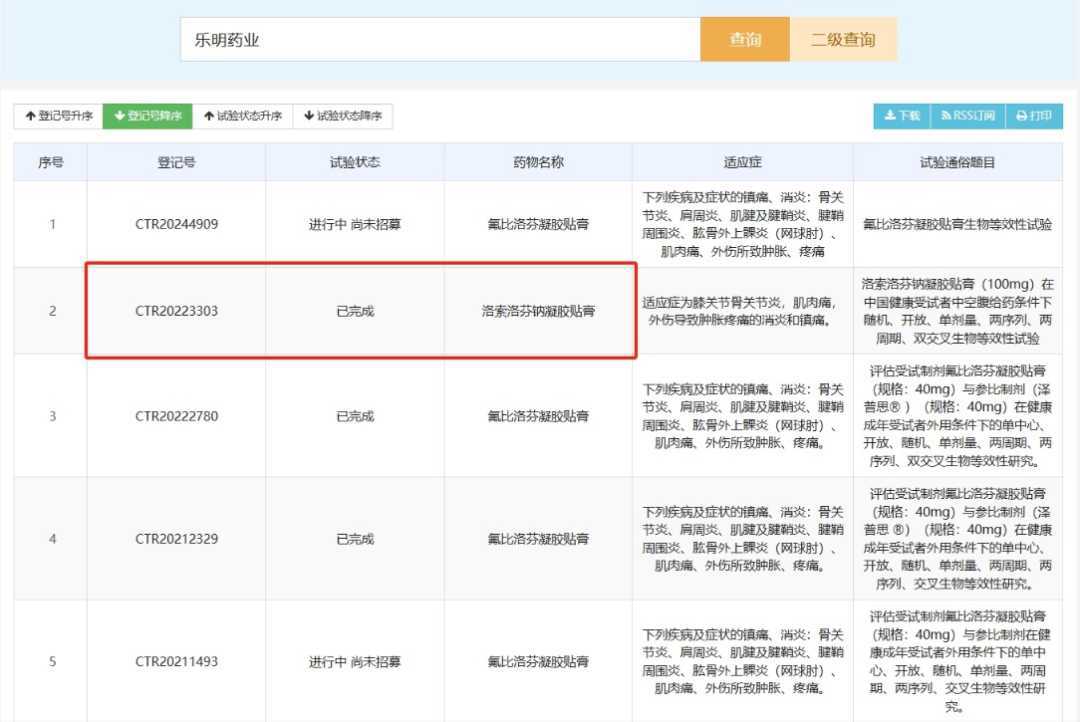
图片来源:药物临床试验登记与信息公示平台
郭新峰指出,乐明药业通过BE申报路径视同通过一致性评价,相较于临床试验,BE药学申报具有成本低、速度快的特点,满足了审评提速的要求。
今年1月3日,国务院办公厅发布的《关于全面深化药品医疗器械监管改革促进医药产业高质量发展的意见》要求提升仿制药质量,并提出将仿制药质量和疗效一致性评价逐步向滴眼剂、贴剂、喷雾剂等剂型拓展。
郭新峰认为,乐明药业洛索洛芬钠凝胶贴膏的获批标志着外用贴膏一致性评价方案趋向统一标准,将吸引更多药企纳入审评并获批。审评提速将吸引更多竞争者入局,当竞争企业数量达到一定规模,如10家左右,且市场空间达到一定水平时,将触发国家集采条件,通过集采为消费者让利,减轻医保负担。然而,他预测至少在短期内,难以满足10家企业获批的条件。
摩熵医药信息显示,目前共有28个洛索洛芬钠凝胶膏/贴膏在进行BE试验,同场竞争的企业包括但不限于北京泰德制药、浙江高跖医药、浙江昂立康制药等,其中多达21个药品试验状态显示“已完成”。
郑重声明:以上内容与本站立场无关。本站发布此内容的目的在于传播更多信息,本站对其观点、判断保持中立,不保证该内容(包括但不限于文字、数据及图表)全部或者部分内容的准确性、真实性、完整性、有效性、及时性、原创性等。相关内容不对各位读者构成任何投资建议,据此操作,风险自担。股市有风险,投资需谨慎。如对该内容存在异议,或发现违法及不良信息,请发送邮件至yxiu_cn@foxmail.com,我们将安排核实处理。











